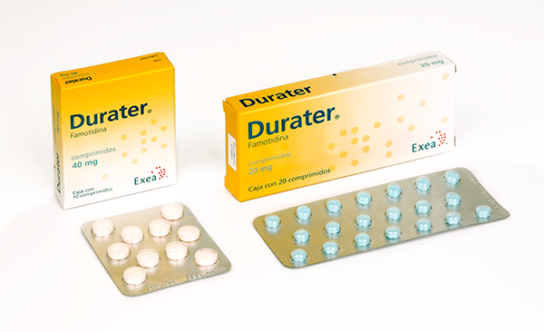
Durater es un antagonista de los receptores H2 de la histamina, cuyo mecanismo de acción es por competencia. En sujetos sanos y en pacientes con úlcera péptica, Durater a razón de 10 - 20 mg por vía oral inhibe en más del 80% la secreción gástrica basal, nocturna y la secreción estimulada por pentagastrina. Doce horas después de la administración de 40 mg por la noche, la secreción basal y la estimulada por pentagastrina se redujo en 70 % y en un 30% respectivamente.
En voluntarios sanos, 40 mg de Durater por las noches inhiben la secreción ácida gástrica nocturna y la estimulada por pentagastrina en forma similar a 300 mg de ranitidina.
Estas dosis de Durater y ranitidina son más potentes que 800 mg de cimetidina.
Después de la administración oral de Durater, la secreción basal de pepsina disminuyó 60% con 10 mg y 72% tras la administración de 20 mg.
En pacientes con úlcera gástrica y duodenal, las concentraciones séricas de gastrina alcanzadas con Durater no difieren de las obtenidas con placebo.
Sin embargo, en voluntarios sanos, 4 horas después de la administración de 20 y 40 mg de Durater las concentraciones séricas de gastrina fueron mayores a las observadas con placebo (p<0.05); pero aún así, se mantuvieron dentro de los límites normales.
Estudios en animales y en humanos han demos- trado que Durater carece de efectos antiandro- génicos (no desplaza a la dehidrotestosterona de su sitio de unión con los andrógenos).
Después de su administración oral, Durater alcanza sus máximas concentraciones plasmáticas en un lapso de 1-3.5 horas.
Con la administración de 40 mg se obtienen niveles de 78 mcg/L. Se requiere una concentración plasmática de 13 mcg/L para inhibir en un 50% la secreción gástrica estimulada. La biodisponibilidad reportada oscila entre un 37 y 45%. El volumen de distribución aparente es de 1.1 a 1.4 L/kg y unión a proteínas es baja, de un 15-22%. Durater se metaboliza en el hígado, dando origen a su metabolito inactivo sulfóxido.
Durater es excretado a través de la orina por filtración glomerular, secreción tubular y por las heces.
De un 25-30% del fármaco es excretado sin cambios. La vida media de eliminación, en pacientes sin deterioro renal es de 2.5-4 horas, pero en pacientes con aclaramiento de creatinina <30 ml/min se incrementa considerablemente.